
LA RECHERCHE N° 306, FÉVRIER 1998
JEAN-POL TASSIN est directeur de recherche à l'Inserm. Il dirige un groupe de recherche au sein de la chaire de Neuropharmacologie du Collège de France, à Paris.
Le terme d'overdose implique souvent une issue fatale, due à l'excès de consommation d'un produit. On pourrait croire que le toxicomane atteint cet extrême parce qu'il est « obligé » de prendre des doses plus élevées pour maintenir un effet satisfaisant. Les observations montrent, cependant, que le toxicomane n'augmente pas ses doses spontanément. Les décès semblent plutôt dus à l'utilisation de mélanges (polytoxicomanie) qui incluent essentiellement, en marge des opiacés et des psychostimulants, l'alcool et les benzodiazépines. Les morts sont aussi liées à la consommation d'un produit d'origine inhabituelle ou, dans le cas des opiacés, à la reprise de la drogue après une longue période d'abstinence. Dans ce dernier cas, le danger vient de ce que la répétition des prises induit une tolérance au produit : une même dose induit des effets moindres. Or, cette tolérance disparaît après une abstinence prolongée. Bien que considérée comme l'une des caractéristiques de la toxicomanie, la tolérance n'est ni nécessaire ni suffisante au déclenchement de la dépendance. Elle paraît tout au plus la faciliter dans la mesure où elle diminue les effets aversifs de la drogue, et permet d'atteindre des doses plus élevées avec un risque moindre. Il existe d'ailleurs des substances non toxicomanogènes qui induisent une tolérance, les anti-hypertenseurs par exemple. Réciproquement, on n'observe pas de tolérance pour les effets psychostimulants des amphétamines.
On a longtemps lié l'installation de la dépendance, chez le toxicomane, à ce qu'il est convenu d'appeler le système de récompense. Il est désormais établi que tous les produits qui déclenchent la dépendance chez l'homme augmentent la libération d'un neuromédiateur, la dopamine, dans une zone précise du cerveau. Il est vraisemblable que l'installation de la dépendance soit due à la modification, par la drogue, de la cinétique et de l'amplitude de cette production de dopamine.
Le toxicomane est assujetti à sa production cérébrale de dopamine
Un homme jeune aux cheveux plutôt longs et aux pupilles bizarres qui, dans un squat délabré, une rue sordide ou un bar enfumé, cherche sa seringue, sa poudre ou son joint, et s'y accroche. Cette image stéréotypée stigmatise l'état de dépendance et la déchéance qui peuvent accompagner la toxicomanie. Malgré un recensement difficile, on considère qu'il existe 200 000 toxicomanes en France. L'essentiel est constitué d'héroïnomanes ; les utilisateurs d'autres produits comme la cocaïne ou les dérivés de l'amphétamine paraissent nettement moins nombreux. Il est probable que tous ne sont pas à proprement parler dépendants, mais aucune enquête ne permet actuellement de connaître la proportion exacte de ceux qui parviennent à contrôler leur consommation, ou même à l'interrompre. Sans parler des substances entraînant elles aussi une dépendance, mais pour lesquelles le phénomène est moins frappant : alcool, tabac, café, par exemple. Et de celles pour lesquelles la dépendance est encore discutée, comme le cannabis (I,II).
Selon la définition donnée en 1981 par l'Organisation mondiale de la santé, la dépendance est « un syndrome pour lequel la consommation d'un produit devient une exigence supérieure à celle d'autres comportements qui avaient auparavant une plus grande importance ». Bien qu'une telle dichotomie stricte ait pu être discutée, on distingue en général la dépendance physique, qui correspond à une réaction de l'organisme à l'absence de produit, de la dépendance psychique, qui a trait aux troubles de l'humeur. Alors que la première disparaît après quelques jours d'abstinence, la seconde peut subsister plusieurs années après l'arrêt de la consommation. L'état de dépendance apparaît progressivement, avec la répétition des prises. Dans sa forme extrême, il se caractérise par un besoin impérieux du produit, qui pousse l'individu à sa recherche compulsive (« craving » pour les anglophones). On parle aussi d'addiction, mot anglo-saxon, lui-même issu d'un terme juridique de vieux français qui signifie devenir esclave pour rembourser ses dettes.
Cerner la dépendance est difficile ; pourtant, les chercheurs disposent d'un atout important. Plusieurs aspects de la conduite des toxicomanes peuvent en effet être reproduits chez l'animal de laboratoire. Chez le rat comme chez l'homme, on peut distinguer nettement dépendance physique et dépendance psychique, les symptômes de cette dernière pouvant être retrouvés chez l'animal même après plusieurs mois d'abstinence.
Dans les années 1980, deux théories ont essayé d'expliquer à la fois pourquoi le toxicomane recherche la drogue de façon compulsive et pourquoi ce besoin ne fait que s'accroître. L'une est bâtie sur la souffrance, l'autre sur le plaisir. Pour les tenants de la première, le toxicomane cherche à compenser les phénomènes de manque qui augmentent au fur et à mesure que les prises se répètent. Cette théorie, dite du « renforcement négatif » - la consommation de la drogue vise à éviter un événement négatif - fut proposée dès 1948 par A. Wikler (1). Elle a été formellement énoncée quarante ans plus tard par Georges Koob et Floyd Bloom du Scripps Research Institute de La Jolla, en Californie (2). Dans une version plus sophistiquée, Richard Solomon, de l'université de Pennsylvanie, a proposé que tout plaisir donne naissance, par réaction, à des sensations de déplaisir qui s'expriment lentement après l'effet euphorisant de la drogue. Et ce déplaisir devient d'autant plus intense que le nombre d'injections ayant engendré du plaisir est élevé (3). De fait, à l'époque où ces hypothèses ont été émises, la plupart des études concernaient les opiacés, comme l'héroïne ou la morphine, pour lesquelles le sevrage entraîne des réactions physiques très pénibles (tremblements, douleurs, diarrhées, sueurs). Mais la théorie présente une faille. En effet, les psychostimulants, dont font partie la cocaïne et les dérivés de l'amphétamine, n'entraînent aucun symptôme de ce type. Ils provoquent pourtant une dépendance psychique au moins aussi puissante que celle due aux opiacés. Même si la sensation physique du manque peut, dans certains cas, pousser le toxicomane à reprendre du produit, elle ne peut donc suffire à expliquer le « craving » et surtout le temps pendant lequel cet état se maintient.
Plutôt que le manque, n'est-ce pas le plaisir procuré par la drogue qui motive le toxicomane ? Cette deuxième hypothèse, dite du « renforcement positif » - la consommation de la drogue vise à répéter un événement positif -, a été formulée au milieu des années 1980. C'est en partie à cause des insuffisances de la première théorie que Jane Stewart puis Roy Wise, deux chercheurs de l'université Concordia à Montréal, se sont intéressés à des expériences pionnières faites dans les années 1950 (4,5,6). J. Olds et P. Milner avaient montré que si l'on place une électrode dans certaines zones précises du cerveau d'un rat, l'animal apprend à appuyer sur une pédale qui, en fermant un circuit électrique, stimule la zone implantée. Le rat s'autostimule ainsi sans interruption. A tel point que si on lui donne le choix entre cette pédale et une autre qui délivre de la nourriture, il choisit la stimulation électrique et s'impose un jeûne fatal. Olds a alors défini un « circuit de la récompense », incluant les zones cérébrales sensibles à ce type de stimulation (7) (fig. 1). Les deux régions les plus réactives sont l'hypothalamus et l'aire tegmentale ventrale. On peut comprendre le rôle crucial de l'hypothalamus dans les sensations de satisfaction lorsqu'on sait que ce centre nerveux est fortement impliqué dans des fonctions comme la faim, la soif ou la sexualité, fondamentales pour le maintien de l'espèce. Quant à l'aire tegmentale ventrale ou ATV, c'est l'une des principales sources de dopamine*, un neuromédiateur cérébral. Les neurones de l'ATV synthétisent la dopamine et la libèrent à distance, dans des aires cérébrales connues pour réguler l'émotivité (septum, amygdale et noyau accumbens). Ce dernier point s'est avéré particulièrement intéressant. Quelques années plus tard, en effet, d'autres chercheurs ont montré que les rats apprennent aussi à « travailler », c'est-à-dire à appuyer sur une pédale ou à mettre leur museau dans un trou, pour recevoir des injections intraveineuses d'amphétamine ou de cocaïne.
Or, ces deux produits augmentent justement la quantité de dopamine dans les cibles de l'ATV (voir l'encadré « Drogues, plaisir et douleur »). La cocaïne et les amphétamines semblaient donc provoquer du plaisir en inondant de dopamine le circuit de récompense. Mais le concept de dépendance était né avec l'héroïne, la morphine et les autres opiacés. Beaucoup de chercheurs les considéraient alors comme les archétypes des substances toxicomanogènes. Or, les opiacés semblaient agir par des mécanismes totalement différents de ceux des psychostimulants. De fait, une certaine rivalité opposait les chercheurs qui s'attachaient à découvrir ce mode d'action, et ceux qui s'obstinaient sur la dopamine. La théorie du renforcement positif est devenue plus plausible lorsqu'il est apparu que les rats apprennent aussi à s'auto-injecter des opiacés en intraveineuse. L'affaire fut entendue en 1988, quand Gaetano Di Chiara et Assunta Imperato, de l'université de Cagliari, en Sardaigne, montrèrent que tous les produits qui déclenchent de la dépendance chez l'homme, comme l'amphétamine et la cocaïne, mais aussi comme la morphine, l'héroïne, la nicotine et l'alcool, augmentent la libération de dopamine dans le noyau accumbens (8). Toutes stimulent donc, par ce biais, le circuit de récompense. Seule ombre au tableau, la théorie du renforcement positif n'expliquait pas pourquoi tous les produits et tous les actes agréables, comme déguster du chocolat ou le simple fait de se nourrir, ne déclenchent pas de dépendance.
Un premier indice vient de ce que la dopamine a un rôle plus complexe que celui d'un simple messager du plaisir. Sa libération peut être déclenchée par la seule présence d'une récompense, même inaccessible. Wolfram Schultz, de l'université de Physiologie de Fribourg, en Suisse, a montré que chez des singes, le contact d'un morceau de pomme active les neurones de l'ATV.
Chez un chat habitué à son environnement, le même effet est obtenu par l'ouverture de la porte de l'animalerie, annonce de l'arrivée de la nourriture. Cette activation des neurones libérant la dopamine s'accompagne d'un changement dans le comportement de l'animal, qui initie un mouvement destiné, selon toute vraisemblance, à atteindre la récompense (9). Dans ce dernier cas, les neurones libérant la dopamine sont donc devenus, par apprentissage, plus réactifs à la signification d'un signal qu'au signal lui-même.
Par analogie, on peut supposer que l'homme constitue au fil des ans une chaîne de signifiants, analogue à une « rose des vents » des plaisirs, autour des neurones à dopamine. C'est, par exemple, le rouge à lèvres qui évoquera la bouche d'une femme, associée elle-même à une satisfaction physique... Les neurones libérant de la dopamine sont d'abord activés par les caractéristiques primaires de la récompense, comme l'odeur, la forme, la texture. Ces divers traits sont progressivement associés à certains signaux de l'environnement. Après l'apprentissage, la seule présence de ces signaux active la libération de dopamine qui, en retour, permet de déclencher un comportement adapté à l'obtention de la récompense.
La dépendance peut s'expliquer si la drogue active artificiellement cette chaîne de signifiants. De fait, chez les rats, après l'injection d'opiacés ou de psychostimulants, l'augmentation du taux de dopamine dans le noyau accumbens est parfaitement corrélée avec le changement du comportement.
L'animal explore sa cage de façon compulsive, activité locomotrice que l'on peut mesurer avec précision grâce à des cellules photoélectriques. Ce regain d'activité est-il lié à la satisfaction apportée par le produit, comme on en a souvent fait l'hypothèse ? On peut plutôt considérer que la drogue, en activant la libération de dopamine, reproduit les signaux qui informent l'animal de l'existence d'une récompense. Le rat se met alors à la rechercher. Et l'effet se renforce au fil des prises. Dès 1973, deux chercheurs de l'université du Michigan, à East Lansing, avaient observé que si l'on injecte à des rats des doses identiques et répétées d'amphétamines, l'activation locomotrice est à chaque injection plus intense (10). On parle de sensibilisation comportementale, ou encore de tolérance inverse, par opposition à la notion classique de tolérance aux drogues, qui veut que l'effet diminue avec les prises (voir l'encadré « Overdose et tolérance »). Ce phénomène a beaucoup intéressé des chercheurs comme Robert Post à Bethesda, dans le Maryland, et Jane Stewart et Paul Vézina, de l'université Concordia à Montréal. Ils ont montré que la sensibilisation comportementale se développe aussi lors de l'injection de cocaïne, d'opiacés et même de nicotine (11-13). Elle s'accompagne d'une hausse des taux de libération de dopamine dans le noyau accumbens, et suit des règles très précises. Elle n'apparaît que si l'animal reçoit son injection dans un environnement inchangé. Surtout, elle se maintient plusieurs mois après la dernière injection. Il existe même une action croisée entre les psychostimulants et les opiacés, l'injection d'un produit de l'un des groupes sensibilisant aux produits de l'autre groupe. La drogue paraît donc, avant tout, mettre en relief l'environnement associé à la récompense.
Jane Stewart et ses collègues n'ont pas manqué de relier ces données aux observations faites chez les toxicomanes. En effet, l'environnement qui entoure les injections revêt, pour eux, une extrême importance. L'une des histoires les plus célèbres est sans doute celle des G.I. du Vietnam chez qui le taux d'héroïnomanie avait atteint un niveau tel, que le gouvernement américain commençait à envisager un programme spécial de désintoxication. Au grand soulagement des autorités, dès que les soldats sont revenus dans leurs familles, le pourcentage de toxicomanes est descendu à un niveau à peine supérieur à celui de la population générale : l'environnement avait changé. A l'inverse, les anecdotes d'héroïnomanes qui rechutent en voyant une seringue, la croix verte de l'enseigne d'une pharmacie (ou même du talc quand il s'agit de cocaïnomanes), sont légion.
La sensibilisation comportementale correspondrait ainsi à une augmentation progressive des associations entre certains éléments saillants de l'environnement et le produit. Un phénomène n'ayant, au bout du compte, que peu de liens avec la satisfaction apportée par la consommation de la drogue. Poussant le raisonnement jusqu'au bout, Terry Robinson et Kent Berridge, de l'université du Michigan, ont remis en cause le lien entre dopamine et plaisir (14). Il faut, selon eux, dissocier la recherche de la drogue de la satisfaction qu'elle procure. Le toxicomane serait surtout affecté d'un désir exacerbé pour le produit, le plaisir qu'il en tire n'étant que secondaire. Il est vrai que la plupart des toxicomanes se plaignent de souffrir de leur besoin permanent de produit, alors que le plaisir ressenti est au mieux identique et souvent plus faible qu'à l'occasion des premières prises. Robinson et Berridge proposent que seule la recherche du produit soit sous le contrôle des neurones libérant la dopamine. Elle correspondrait à la sensibilisation comportementale observée chez l'animal. Quant au plaisir, il serait médié par d'autres voies nerveuses.
La théorie est séduisante. Elle ne permet cependant pas de comprendre pourquoi consommer de la drogue apporte, malgré tout, du plaisir au toxicomane. Des éléments de réponse peuvent être trouvés dans une série d'expériences réalisées sur le singe par Wolfram Schultz (fig. 2) (15). Ces expériences introduisent une notion essentielle, celle d'un niveau de base dans l'activité des neurones à dopamine. Dans un premier temps, le singe reçoit une récompense sous la forme d'une petite quantité de jus de pomme, ce qui a pour effet d'activer ces neurones.
Dans une seconde expérience, le singe a appris qu'une petite lumière précède la récompense. Les neurones sont alors activés lorsque la lumière apparaît, leur activité revenant au niveau initial à l'arrivée de la récompense. Troisième situation, lorsque la lumière s'allume sans être suivie de jus de pomme, l'activité des neurones diminue au moment où la récompense est attendue.
Ainsi, dans une situation « naturelle », l'activité des neurones libérant la dopamine dépasse le niveau de base lorsqu'apparaît le signal précurseur, pour retourner au niveau antérieur au moment de la récompense. Si cette dernière n'est pas obtenue, l'activité neuronale descend au-dessous du niveau de base. Ce phénomène s'expliquerait, au plan neurobiologique, par l'absence de retour d'information vers les neurones libérant la dopamine. Quand la récompense est obtenue, l'hypothalamus, dont on a vu qu'il joue un rôle central dans des fonctions comme la faim et la soif, enverrait un message d'activation en direction des neurones libérant la dopamine. Si la récompense attendue ne vient pas, l'absence de retour en provenance de l'hypothalamus entraînerait la baisse d'activité des mêmes neurones. On peut supposer que c'est cette baisse momentanée de dopamine qui est associée au mal-être.
La drogue bouleverse cet équilibre. En situation normale, la fluctuation de l'activité des neurones libérant la dopamine dure de une à deux secondes. Les satisfactions naturelles sont assujetties à cette cinétique et ne la modifient pas. En revanche, les produits toxicomanogènes agissent directement sur les neurones libérant la dopamine, et cette action se compte en dizaines de minutes. La cinétique du phénomène est donc complètement perturbée par les drogues. Pendant la large fenêtre de temps durant laquelle les taux de dopamine sont ainsi artificiellement élevés, tous les éléments de l'environnement, ainsi que les sensations psychiques, sans discrimination, peuvent être associés à la récompense. La dépendance se maintient des mois voire des années, même en l'absence de drogue, parce qu'il y a mémorisation des associations.
Selon cette nouvelle hypothèse, le seuil autour duquel fluctue l'activité des neurones libérant la dopamine est fondamental dans l'attitude face aux drogues. C'est en fonction de lui, que le cerveau recherche la récompense et ressent la satisfaction - lorsqu'il est au- dessus du seuil - ou le manque - en dessous du seuil. D'une certaine façon, ce seuil peut être considéré comme un index du « niveau thymique » que les psychiatres utilisent pour définir l'humeur d'un individu. Il est peu probable qu'un tel seuil soit défini dans l'absolu. Une analogie intéressante peut être faite avec la douleur. Récemment, Francis Colpaërt, des laboratoires Pierre Fabre à Castres, a proposé que l'évaluation de l'intensité d'une douleur se ferait en prenant comme référence les informations sensitives qui ont précédé la sensation douloureuse (16).
De même, le niveau thymique d'un individu dépendrait, entre autres, de l'intégration des activités des neurones libérant la dopamine dans les heures, les jours, voire les années qui précèdent. La base de ce seuil, propre à chacun d'entre nous, se constituerait au cours des premières années du développement. Mais celui-ci serait ensuite modulé en permanence par tous les paramètres internes et externes auxquels est soumis l'individu. Toute situation, toute pensée consciente ou inconsciente, conduisant le système à se trouver au-dessous de ce seuil déclencherait, d'une part une sensation de mal-être, d'autre part une activité motrice ou psychique susceptible de ramener l'ensemble à un niveau acceptable. On retrouve ici l'importance du manque qui était mis en avant dans la théorie du renforcement négatif. Néanmoins, dans notre hypothèse, ce manque pourrait s'assimiler à un phénomène d'ordre psychique. Un tel manque est théoriquement repérable par des techniques neurobiologiques, puisqu'il se traduirait par une baisse globale de libération de dopamine. Pour qu'il y ait satisfaction, ou tout au moins pour que la sensation désagréable disparaisse, le système doit au moins atteindre et éventuellement dépasser le seuil. Qui plus est, tout comportement entraînant le système trop au-dessus du seuil aura pour conséquence de l'augmenter, puisqu'il sera pris en compte dans l'évaluation du futur seuil. Par la suite, l'obtention de nouvelles satisfactions nécessitera alors un effort plus important.
Cette notion de seuil relatif, dépendant à la fois des événements antérieurs et des réactions du cerveau à l'environnement immédiat, permet de mieux comprendre l'installation de la dépendance. L'ingestion de produits toxicomanogènes est effectivement susceptible de déclencher des sensations de bien-être, mais aussi d'augmenter le seuil ; et l'élévation chronique du seuil augmente évidemment, à moyen terme, la probabilité de se trouver en dessous. Ce qui poussera à rechercher à nouveau la drogue.
Il n'est pas exclu que des pathologies mentales en relation avec la dopamine, en particulier certaines dépressions, soient la cause ou la conséquence de l'élévation de ce seuil. De fait, un très grand nombre d'antidépresseurs agissent directement ou indirectement sur la libération de dopamine, mesurée principalement dans le noyau accumbens. Une partie des situations de dépendance ne seraient ainsi, à bien des égards, que le reflet de pathologies dépressives préexistantes. Il n'est pas exclu que les antidépresseurs agissent sur le seuil en influençant la boucle de contrôle de l'activité des neurones à dopamine.
De fait, tous les individus qui utilisent de la drogue ne deviennent pas nécessairement dépendants. Il existe donc des vulnérabilités individuelles ou des processus de protection vis-à-vis de la toxicomanie. Cette variabilité se retrouve d'ailleurs chez les animaux. Lorsqu'on injecte de l'amphétamine à des rats, une proportion faible mais constante d'entre eux ne montrent que très peu de changements dans leur comportement. D'autres ne développent jamais de tolérance inverse. Une part est bien sûr innée : la sensibilité aux drogues des neurones libérant la dopamine diffère probablement d'une personne à l'autre. Mais la susceptibilité dépend aussi de l'histoire de l'individu, en particulier des situations plus ou moins conflictuelles qu'il a pu rencontrer au cours de son existence. De cette histoire individuelle dépend le seuil dont nous avons parlé. Le stress active la libération de dopamine et, selon toute vraisemblance, des stress chroniques augmentent ce seuil. Qui plus est, Pier Vincenzo Piazza et Hervé Simon, de l'université de Bordeaux, ont montré que les sécrétions de corticoïdes induites par le stress augmentent la réactivité des neurones libérant la dopamine aux produits toxicomanogènes (17).
Il est clair que, même si la dopamine représente un maillon fondamental dans la dépendance, elle n'est pas seule à intervenir. Au laboratoire, nous avons montré, avec Laurent Darracq et Gérard Blanc, que l'augmentation de la libération de dopamine dans le noyau accumbens n'avait de conséquence comportementale que si certains neurones du lobe frontal du cortex étaient stimulés par un autre neuromédiateur, la noradrénaline (18,19). Nous avons émis l'hypothèse que cette dernière participe à la synchronisation de l'activité des neurones produisant la dopamine. C'est la libération simultanée de dopamine, dans différentes zones d'une même structure, qui permettrait alors son action fonctionnelle.
Avec la répétition des prises dans un environnement identique, la libération de dopamine augmente, et le lien qui soude la satisfaction ressentie aux conditions d'obtention du produit se consolide. La drogue et les conditions de sa prise deviennent alors la seule solution à toute baisse du niveau thymique au-dessous d'un certain seuil, qui lui-même dépend de l'histoire de l'individu. C'est le caractère exclusif du recours à la drogue qui peut expliquer la dépendance. Le toxicomane a progressivement éliminé toutes les autres solutions.
P.G. Strange, Brain biochemistry and brain disorders , Oxford University Press, Oxford, 1992.
F. Trovero, S. Pirot, J.-P. Tassin, F. Facy, Drogues et toxicomanies : Neurobiologie, Epidémiologie , Dossiers documentaires, Inserm/ Nathan, Paris, 1993.
S AS Infos. Ce journal trimestriel (5 numéros parus) analyse des rapports officiels et publie des enquêtes sur la toxicomanie. 247 rue de Belleville, 75019 Paris.
NEUROBIOLOGIE

Salvador Dali, Le phénomène de l'extase, 1933. Le cerveau associe naturellement l'euphorie ressentie dans un contexte donné à une chaîne de signifiants : formes, odeurs... La dopamine paraît jouer un rôle central dans ce processus. (Cliché Descharnes & Descharnes, collection particulière © ADAGP 1998)

Figure 1. Le circuit de « récompense » cérébral, tel qu'il a été défini chez l'animal. En situation « naturelle », le circuit fonctionnerait de la façon suivante. L'arrivée d'un signal annonçant une récompense, après traitement sensoriel par le cortex, modifie l'activité de certains neurones de l'aire tegmentale ventrale. Ceux-ci libèrent de la dopamine dans le septum, le noyau accumbens, l'amygdale et le cortex préfrontal (flèches vertes). Le noyau accumbens intervient dans l'activation motrice de l'animal. Le cortex préfrontal est impliqué dans la focalisation de l'attention. Toutes ces cibles sont interconnectées et innervent l'hypothalamus (flèches rouges), l'informant de la présence d'une récompense. Chaque structure cérébrale participerait ainsi, pour sa part, aux aspects moteurs, cognitifs et affectifs de la réponse.
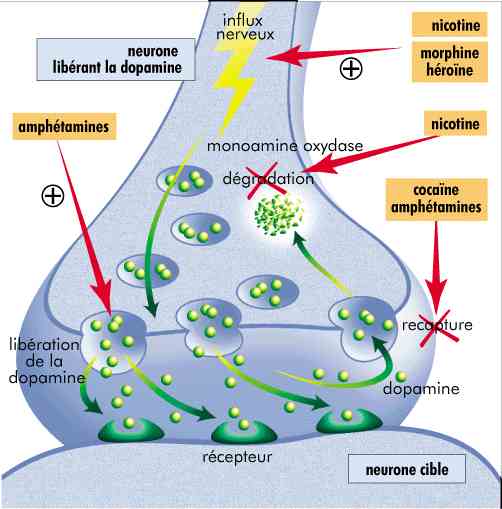
Zone de contact ou synapse entre le neurone qui produit la dopamine (neurone-émetteur) et le neurone cible. La dopamine est libérée dans le fin espace entre les deux neurones (fente synaptique). Elle agit en se fixant sur des récepteurs portés par le neurone cible. La dopamine est ensuite recaptée par le neurone émetteur et détruite par une enzyme, la monoamine oxydase.

Figure 2. L'activité de neurones de l'aire tegmentale ventrale a été enregistrée chez le singe dans trois situations successives. On voit sur le schéma central que dans un deuxième temps, la seule annonce de la récompense (signal lumineux) suffit à libérer la dopamine. Lorsqu'on supprime la récompense en conservant l'annonce, l'activité des neurones diminue de façon transitoire. (D'après réf. (15))
*LA DOPAMINE
(dopa vient de dihydroxyphénylalanine et non de l'anglais dope...) est une substance chimique de la famille des catécholamines. Elle est essentiellement produite par les neurones de deux structures cérébrales : l'aire tegmentale ventrale et la substance noire. La première intervient sur le « circuit de récompense ». La deuxième participe au contrôle de la motricité : la maladie de Parkinson est due à sa dégénérescence. La dopamine intervient aussi dans d'autres fonctions : mémoire de travail, focalisation de l'attention...
NOTES
(1) A. Wikler, Am. J. Psychiatry, 105, 329, 1948.
(2) G.F. Koob et F.E. Bloom, Science, 242, 715, 1988.
(3) R.L. Solomon, « Acquired motivation and affective opponent-processes », in J. Madden (Ed.) Neurobiology of Learning. Emotion and Affect, Raven Press, New York, 1991, p. 307-348.
(4) J. Stewart et al., Psychol. Rev., 91, 251, 1984.
(5) R.A. Wise, Annu. Rev. Neurosci., 19, 319, 1996.
(6) J. Olds, P.M. Milner, J. Comp. Physiol. Psychol., 47, 419, 1954.
(7) J. Olds, Sci. Am., 195, 105, 1956.
(8) G. Di Chiara et A. Imperato, Proc. Natl. Acad. Sci. USA, 85, 5274, 1988.
(9) B.L. Jacobs, « Overview of the activity of brain monoaminergic neurons across the sleep-wake cycle », in Sleep : neurotransmitters and neuromodulators, A. Wauquier et al. (eds), Raven Press, New York, 1985, p. 1-14.
(10) H.A. Tilson, R.A. Reich, Pharmacol. Biochem. Behav., 1, 149, 1973.
(11) R.M. Post et al., « Conditioned sensitization to the psychomotor stimulant cocaine » in P.W. Kalivas et H.H. Samson (Eds), Annals of the New York Academy of Sciences : the Neurobiology of Drug and Alcohol Addiction, The New York Academy of Sciences, New York, 1992, p. 386-399.
(12) P.W. Kalivas, J. Stewart, Brain Res. Rev., 16, 223, 1991.
(13) P. Vezina, J. Stewart, Brain Res., 516, 99, 1991.
(14) T.E. Robinson, K.C. Berridge, Brain Res., 18, 247, 1993.
(15) W Schultz et al., Science, 275, 1593, 1997.
(16) F.C. Colpaërt, Pharmacol. Rev, 48, 355, 1996.
(17) P.V. Piazza et al., Brain Res., 658, 259, 1994.
(18) G. Blanc et al., Europ. J. Neurosci., 6, 293, 1994.
(19) L. Darracq et al., J. Neurosci ., sous presse.
(20) E.D. French, Neuroscience Letters, 226, 159, 1997.
(21)G. Tanda et al., Science, 276, 2048, 1997.
(22)S.W. Johnson, R.A. North, J. Neurosci ., 12, 483, 1992.
La Recherche a publié :
(I) Jean-Pol Tassin, Nicolas Witkowski, « Cannabis : un stupéfiant à démystifier », mai 1996.
(II) Ingrid Wickelgren, « Le cannabis, une drogue comme les autres », octobre 1997.