
- C'est lors de la campagne d'Egypte que les médecins français découvrirent les propriétés psychoactives du chanvre, et l'usage qui en était fait. On l'incorporait dans du miel, mais on pouvait aussi le fumer seul ou avec du tabac. (Femmes d'Alger dans leur appartement, Delacroix, huile sur toile, cliché RMN/ARNAUDET)
Les effets du cannabis dévoilent de nouvelles propriétés de notre cerveau
Le cannabis : de la drogue au médicament
Daniele Piomelli
DANIELE PIOMELLI est professeur au département de pharmacologie de l'université de Californie, Irvine, aux Etats-Unis.
La Recherche n°323, septembre 1999
De retour à Paris après la campagne d'Egypte, M. Rouyer, pharmacien ordinaire de l'armée napoléonienne et membre de la Commission des sciences et des arts, rédigea pour le Bulletin de pharmacie un mémoire sur les plantes employées dans la médecine populaire de ce pays. Une place importante dans ce bref exposé, publié en 1810, était occupée par le chanvre (Cannabis sativa, L.) , dont les propriétés étaient encore très mal connues des médecins européens.
« Le chanvre, écrit-il, est selon les Egyptiens la plante par excellence, non pour les avantages qu'on en tire en Europe et dans beaucoup d'autres pays [la fabrication de cordes et tissus], mais à cause des singulières propriétés qu'ils lui attribuent. Celui qu'on cultive en Egypte est enivrant et narcotique. On se sert des feuilles et des sommités de cette plante, qu'il faut cueillir avant la maturité : dans cet état, on en fait une conserve qui sert à composer le berch, le diasmouk, le bernaouy. Les feuilles de chanvre réduites en poudre et incorporées dans du miel, ou délayées dans l'eau, font la base du berch des pauvres. Ceux-ci s'enivrent encore en fumant le chanvre seul, ou mêlé avec le tabac : on en fait une grande consommation en Egypte, où on ne le cultive que pour cet usage. »
Cette description des propriétés psychoactives du chanvre, une des premières en Europe depuis Hérodote, corroborait les conclusions du Mémoire sur la dynastie des assassins et sur l'origine de leur nom, que Sylvestre de Sacy avait lu l'année précédente à l'Académie des inscriptions et belles-lettres.
Nouvelle mode. En s'appuyant sur des arguments philologiques*, de Sacy avait suggéré que la mystérieuse substance hallucinogène employée par la secte musulmane des Hashishiyya au cours de ses cérémonies mystiques pourrait correspondre au chanvre, dont il avait aussi décrit les effets euphorisants et psychotropes.
Après des siècles d'oubli et d'indifférence, sciences naturelles et philologie se rejoignirent donc pour montrer au public des nations occidentales que l'esprit humain - res cogitans et siège de l'âme - pouvait être altéré d'une façon spectaculaire par l'ingestion d'une simple plante. Dans l'intervalle de quelques années, une avalanche de romans, de contes et d'essais, où le haschisch jouait un rôle tantôt de protagoniste, tantôt de comparse, alla s'ajouter à ceux qui, dans la même période, étaient écrits sur une autre drogue d'origine végétale, l'opium.
Premières études. Si Charles Baudelaire, grand témoin de cette fascination littéraire, ne fut peut-être qu'un spectateur critique des actions du haschisch, son contemporain Jacques Joseph Moreau de Tours, médecin à Bicêtre, théorisa que seule une expérience personnelle de cette drogue permet d'en saisir la nature complexe (voir l'encadré ci-après). Dans la préface à son traité Du haschisch et de l'aliénation mentale, paru en 1845, il affirme : « L'expérience personnelle est ici le critérium de la vérité. Je conteste à quiconque le droit de parler des effets du haschisch, s'il ne parle en son nom propre, et s'il n'a été à même de les apprécier par un usage suffisamment répété. »
Que l'on souscrive ou pas à cet avis, il est indéniable que Moreau a été le premier à proposer une théorie psychologique des effets de cette drogue. Selon lui, nous vivons dans le présent grâce à un acte de volonté qui dirige notre attention vers tous les objets et les phénomènes qui ont pour nous un intérêt actuel. Le haschisch, en affaiblissant la volonté - c'est-à-dire en réduisant la force intellectuelle qui domine les idées, les associe et les relie - laisse libre cours aux souvenirs et à l'imagination. Passé et futur prennent alors le dessus sur le présent, provoquant un état de dissociation d'idées qui, d'après Moreau, n'est pas seulement un symptôme primaire du cannabisme, mais aussi un « fait primordial » à la base de toute aliénation mentale.
Les paradis artificiels« C'est d'abord une certaine hilarité, saugrenue, irrésistible, qui s'empare de vous. Ces accès de gaieté non motivée, dont vous êtes presque honteux, se reproduisent fréquemment et coupent des intervalles de stupeur pendant lesquels vous cherchez en vain de vous recueillir. Les mots les plus simples, les idées les plus triviales prennent une physionomie bizarre et nouvelle [...]. Des ressemblances et des rapprochements incongrus, impossibles à prévoir [...] jaillissent dans votre cerveau [...]. Bientôt les rapport d'idées deviennent tellement vagues, le fil conducteur qui relie vos conceptions si tenues, que vos complices seuls peuvent vous comprendre [...] la bienveillance tient une assez grande place dans les sensations causées par le haschisch ; une bienveillance molle, paresseuse, muette, et dérivant de l'attendrissement des nerfs. » Charles Baudelaire, 1860. |
L'importance que Moreau attribue au dérapage des processus attentionnels causé par le haschisch est certainement justifiée, comme nous le verrons plus tard ; son hypothèse que maladie mentale et intoxication cannabique possèdent des éléments communs est aussi captivante. Mais l'élève de Philippe Pinel*, en se concentrant sur les effets psychotropes du cannabis, négligea d'autres propriétés pharmacologiques importantes de cette plante. Celles-ci n'échappèrent pas au médecin anglais Robert Christinson, qui les discuta dans son Commentaire à la pharmacopée britannique et américaine , publié en 1848. « Dans mon expérience professionnelle, écrit-il, le cannabis a provoqué le sommeil, soulagé la douleur et arrêté les spasmes musculaires ; je n'ai pas remarqué d'effet désagréable durant ou après son action... Dans l'ensemble, il s'agit d'un médicament qui mérite des études plus approfondies. »
Symptômes. L'essentiel des effets exercés par le cannabis sur l'organisme humain, a été décrit par Moreau et par Christinson. Comment les décrire à la lueur de nos connaissances actuelles ? Les symptômes de l'intoxication cannabique sont d'abord de nature périphérique, c'est-à-dire extracérébrale : un profond élargissement des vaisseaux sanguins (qui entraîne une baisse de la tension artérielle), accompagné par une dilatation de la musculature bronchiale (qui cause à son tour une facilitation de la fonction respiratoire). La nature psychoactive de la drogue - cet ensemble de phénomènes qu'aux temps de Moreau on appelait la fantasia et, de nos jours, le high - se manifeste dès qu'elle atteint le système nerveux central (SNC). Les mouvements deviennent alors plus lents et difficiles ; la sensibilité aux couleurs, aux saveurs et à la musique, s'aiguise ; la mémoire des événements récents s'affaiblit ; l'individu est saisi par une euphorie souvent très marquée, tout en restant conscient de son état d'intoxication ; la notion du temps est perturbée ; les spasmes musculaires et la douleur sont soulagés. A des doses très élevées, la prise de cannabis peut aussi provoquer de véritables hallucinations, qui consistent, comme l'avait déjà remarqué Théophile Gautier, surtout en des distorsions de la perception du corps et de l'espace. Le cannabis inhiberait également la réponse immunitaire et réduirait le transit intestinal (fig. 1). La toxicité aiguë du cannabis est très limitée, ses modestes effets toxiques (tolérance, perte de motivation) ne se révélant qu'à la suite d'un usage chronique. L'Académie des sciences écrit prudemment à ce propos : « La toxicité générale du cannabis [...] bien que faible, [...] ne peut être considérée comme dénuée de conséquence à plus ou moins long terme (1) ». Quant au pharmacologiste Bernard Roques, il écrivait dans son récent rapport au secrétariat d'Etat à la Santé « La toxicomanie au cannabis n'entraîne pas de neurotoxicité telle qu'elle a été définie [...] par des critères neuroanatomiques, neurochimiques et comportementaux(2) ».
Que les différentes facettes de l'intoxication cannabique fussent causées par un constituant actif présent dans les feuilles et dans les fleurs du chanvre était déjà soupçonné par Moreau et par Christinson, qui avaient été témoins de l'isolement d'autres substances psychoactives d'origine végétale (morphine, nicotine, etc.). Mais la caractérisation du composant actif du chanvre se révéla très ardue : il fallut attendre en effet plus d'un siècle - les études de Roger Adams dans les années 1940 et celles de Raphaël Mechoulam vingt ans plus tard - pour arriver à établir d'une façon définitive la structure chimique de ce composé évasif(3). Le D9-tetrahydrocannabinol (THC) fut alors reconnu, parmi des centaines de composés présents, comme le principal responsable de l'activité pharmacologique du chanvre.

- Figure 1. Le cannabis n'est pas exclusivement psychoactif. Ses effets périphériques ont intéressé les médecins du XIXe siècle, avant d'être oubliés, puis étudiés à nouveau aujourd'hui. Cependant, le pharmacologistes ne parviennent pas à dissocier les effets sur cerveau de ceux concernant les autres organes.
Molécule originale. La nature unique de cette activité se manifeste déjà au niveau de la structure chimique du THC. Les constituants actifs contenus dans la plupart des plantes psychotropes, telles la cocaïne (extraite des feuilles de coca, Erythroxylon coca) ou la morphine (extraite de l'opium, Papaver somniferum), sont des substances alcaloïdes. Elles présentent une charge positive très faible et forment, par conséquent, des sels qui se dissolvent sans difficulté dans le sang et dans les autres solutions qui entourent nos organes intérieurs.
Le THC, au contraire, est un composé fortement lipophile qui se dissout beaucoup plus facilement dans les graisses - comme celles qui forment les membranes cellulaires - que dans l'eau. Cette propriété a joué un rôle assez surprenant dans l'histoire du THC. Mais, pour pouvoir apprécier pleinement ce rôle, il faut d'abord considérer brièvement le mécanisme d'action des agents psychoactifs. Prenons en exemple la morphine, dont on connaît bien les puissants effets analgésiques et narcotiques.
Une fois entrée dans la circulation sanguine, la morphine franchit la barrière qui sépare le sang du cerveau et pénètre dans le système nerveux central. Là, elle interagit avec une fraction très limitée de cellules nerveuses : celles qui possèdent sur leur surface extérieure des protéines reconnaissant exactement sa forme, comme une serrure reconnaît sa propre clé. La liaison temporaire avec ces protéines (appelées récepteurs opioïdes) déclenche une série de réactions biochimiques à l'intérieur des cellules, qui changent leurs propriétés électriques et entraînent les effets pharmacologiques de la drogue.
A partir de l'isolement du THC et jusqu'à la fin des années 1980, l'opinion prévalente parmi les scientifiques était que le THC ne pourrait pas interagir avec un récepteur à cause de son affinité pour les graisses ; on pensait plutôt que cette molécule changeait la fluidité de la membrane cellulaire d'une façon non sélective. A cette théorie du THC comme « savon neuronal » un petit groupe de chercheurs opposa une objection dictée par l'esprit d'observation et le bon sens : si le mécanisme d'action du THC est purement physico-chimique, demandaient-ils, pourquoi ses effets sont, au contraire, si uniques ? Pourquoi le THC n'aurait-il pas, comme la morphine, sa propre « serrure » ?
Cette hypothèse gagna du terrain lorsque, en 1988, Allyn Howlett et ses collaborateurs à l'université de Saint Louis (Etats-Unis) montrèrent que la liaison de différents dérivés du THC aux membranes de cellules de cerveau suivait des critères très rigides. Un petit changement de structure chimique entraînait des modifications importan-tes dans la capacité à s'associer aux membranes, un phénomène explicable seulement par l'interaction avec un récepteur sélectif. Bientôt, d'autres expériences confirmèrent cette conclusion. Miles Herkenham, un neuroanatomiste aux National Institutes of Health (NIH) de Bethesda (Etats-Unis), démontra que le THC se lie uniquement aux régions du cerveau qui sont impliquées dans ses effets psychotropes : le cortex (euphorie, dérangement des processus attentifs), l'hippocampe (affaiblissement de la mémoire à court terme), le striatum (réduction de l'activité motrice, perte de la notion du temps) et le cervelet (troubles de la coordination motrice).
Néanmoins, la preuve irréfutable de l'existence d'un récepteur cannabinoïde dut attendre l'essor d'une méthode de biologie moléculaire connue sous le nom de clonage par homologie. Cette technique permet d'isoler les gènes de nouveaux récepteurs à partir de la structure d'un récepteur connu, en tirant profit des ressemblances génétiques qui existent entre les membres d'une même famille de protéines. En d'autres termes, elle consiste à « pêcher » des récepteurs en utilisant un morceau d'ADN comme appât. Comme à la pêche, d'ailleurs, on ne peut pas toujours prévoir ce qu'on va attraper, et il arrive souvent d'isoler des récepteurs dont on ne connaît ni la molécule activatrice ni l'utilité.
Composé endogène. C'est justement ce qui arriva à une collègue de Miles Herkenham aux NIH, Lisa Matsuda. Au cours d'une recherche concentrée sur les récepteurs d'une famille de protéines appelées tachykinines, la scientifique isola un de ces récepteurs sans fonction. Au lieu d'abandonner son « orphelin » dans un congélateur, elle décida de se mettre en quête du médiateur chimique responsable de son activation.
On raconte qu'un jour, après avoir essayé sans succès une longue liste de composés, elle passa devant le bureau de Herkenham. Affichée sur la porte du neuroanatomiste, il y avait une photographie de la localisation des sites de liaison du THC dans le cerveau du rat. Matsuda sursauta : la distribution du récepteur qu'elle avait isolé correspondait comme deux gouttes d'eau à celle du THC. A ce point, une ou deux expériences pharmacologiques furent suffisantes pour prouver que son « orphelin » était la serrure longuement cherchée : le récepteur cannabinoïde(4).
Si la fonction d'un récepteur est de capter les messages chimiques qu'une cellule nerveuse envoie à une autre, quel peut être le rôle d'un récepteur qui reconnaît, à l'intérieur de notre corps, un métabolite produit par une plante ? La question serait plus aisée s'il s'agissait d'une phéromone ou d'un composé odorant, mais comment y répondre dans le cas d'une substance psychoactive ?
En excluant l'hypothèse que l'évolution ait prévu la beat generation, reste celle que le récepteur cannabinoïde reconnaisse la molécule du THC parce qu'il la prend pour une autre : c'est-à-dire pour un composé endogène qui, produit et libéré dans le cerveau, entraîne des réponses physiologiques semblables à celles du cannabis. Mais, si une telle substance existe, comment peut-on en démontrer l'existence ?
En théorie, c'est simple. Il suffit de prendre le cerveau d'un animal, préparer un extrait cellulaire et séparer ses différents composants chimiques. Ensuite, il suffit d'établir si, parmi ces composants, il y en a un qui se lie spécifiquement au récepteur du THC et d'élucider sa structure. Cependant, le cerveau d'un mammifère contient des millions de molécules différentes, ce qui rend la substance cannabinoïde endogène aussi difficile à trouver que la proverbiale aiguille dans la botte de foin.
La bonne formule. Il faut donc avoir une bonne idée, beaucoup de chance et énormément de patience. William Devane, un jeune chercheur américain qui avait déjà collaboré avec Allyn Howlett à la découverte du récepteur cannabinoïde, eut à la fois la bonne idée et la détermination nécessaire pour la poursuivre. Son raisonnement était simple : si le récepteur du THC reconnaît une substance lipophile, c'est probablement parce que son activateur endogène a les mêmes propriétés chimiques. La substance cannabinoïde endogène serait donc, elle aussi, lipophile. Si cette hypothèse est correcte, l'isolement de cette substance hypothétique devrait être plus facile, car un extrait de composés lipidiques contient, naturellement, un nombre plus limité de molécules qu'un mélange de protéines, lipides et hydrates de carbone. En développant son idée, Devane s'embarqua dans un avion pour Jérusalem et alla travailler dans le laboratoire de Raphaël Mechoulam.
En 1992, au bout de deux années d'expériences et après avoir manipulé des centaines de cerveaux de porc, Devane isola quelques milligrammes d'un composé qui s'associait d'une façon sélective au récepteur cannabinoïde cérébral(5). La quantité qu'il avait isolée était minuscule, mais suffisante pour établir la composition de la molécule inconnue, à l'aide de techniques de résonance magnétique et de spectrométrie de masse.
Hypothèse. Son hypothèse de départ se révéla exacte. Le composé cannabinoïde endogène était effectivement une molécule lipophile, bien que douée d'une structure chimique très différente de celle du THC : la longue chaîne d'un acide gras polyinsaturé (proche d'une autre classe de lipides bioactifs, les eicosanoïdes) y était condensée avec une molécule d'éthanolamine (fig. 2). Puisque l'acide gras en question s'appelle acide arachidonique, le nom chimique de la substance cannabinoïde endogène est arachidonyl-ethanolamide ; mais Devane, qui a un faible pour la culture indienne, préféra la baptiser anandamide, du sanskrit ananda, « félicité » (voir l'encadré ci-après).
Quelles cellules produisent l'anandamide, et comment ? Quels stimuli déclenchent sa formation, et dans quelles circonstances ? Quels sont les rôles de l'anandamide dans la fonction cérébrale ?

- Figure 2. Le THC, composé actif du cannabis, et l'anandamide, le cannabinoïde présent naturellement dans notre cerveau, possèdent des formules chimiques très différentes. Ils se lient cependant sur les mêmes récepteurs. Le nom chimique de l'anandamide est arachidonyl-ethanolamide.
Un deuxième cannabinoïde endogèneTrois ans après la découverte de l'anandamide, Takayuki Sugiura à l'université de Teikyo au Japon et Raphaël Mechoulam à l'université de Jérusalem proposèrent l'existence d'une autre substance cannabinoïde endogène. Les deux groupes montrèrent que le 2-arachidonylglycerol (2-AG), un dérivé de l'acide arachidonique dont la structure chimique ressemble beaucoup à celle de l'anandamide, était capable de se lier aux récepteurs cannabinoïdes et de reproduire les effets pharmacologiques du THC. Malgré ses ressemblances structurales avec l'anandamide, le 2-AG est produit par l'activation d'une voie biochimique différente.  On en sait encore très peu sur les rôles physiologiques du 2-AG. Nephi Stella, dans notre laboratoire, et Paul Schweitzer (au Scripps Research Institute) ont montré que la production de ce composé est stimulée par l'activité de fibres nerveuses qui sécrétent du glutamate - un neurotransmetteur impliqué dans les processus de formation de la mémoire. Une fonction physiologique du 2-AG pourrait donc être le réglage de ces processus, peut-être par l'inhibition des effets du glutamate. |
Faire une expérience scientifique signifie tout d'abord imaginer un morceau de réalité possible, que les manipulations et les données expérimentales nous permettent de considérer, plus que possible, probable. Quel scénario pourrions-nous donc envisager ? Tout d'abord, une cellule nerveuse, stimulée, libère l'anandamide dans le milieu extracellulaire. Là, l'anandamide prend contact avec des cellules qui présentent sur leur membrane le récepteur cannabinoïde.
Ce dernier transmet la nouvelle que la liaison a eu lieu en changeant sa forme et en obligeant d'autres protéines qui lui sont proches à faire de même. Le message passe ainsi à l'intérieur de la cellule, qui modifie ses propriétés biochimiques et électriques, selon sa localisation dans le cerveau et ses fonctions physiologiques. Une fois sa tâche terminée, l'anandamide est rapidement éliminée : ses effets disparaissent pour faire place à un nouveau cycle de neurotransmission.
Plusieurs données expérimentales confirment ces prédictions. Les travaux menés dans notre laboratoire (d'abord au sein de l'unité 109 de l'INSERM, dirigée par Jean-Charles Schwartz, et puis au Neurosciences Institute de San Diego) ont reconstruit les étapes principales du mécanisme de formation de l'anandamide(6).
A la différence d'autres médiateurs neuronaux, tels que la dopamine et les neuropeptides, l'anandamide n'est pas emmagasiné dans les vésicules synaptiques, ces sachets microscopiques qui sécrètent leur contenu de neurotransmetteurs dans l'espace entre un neurone et un autre. Au contraire, l'anandamide est produit sur demande par clivage enzymatique d'un précurseur présent dans la membrane du neurone (fig. 3). Le processus d'inactivation de l'anandamide, étudié dans notre laboratoire, est assuré par un double mécanisme de recapture et de dégradation enzymatique : une protéine spécialisée dans la fonction de transport reconnaît l'anandamide extracellulaire, tout comme le ferait un récepteur, et la véhicule à l'intérieur de la cellule où elle est détruite par une enzyme ad hoc (7).
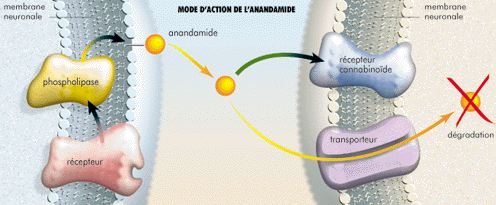
- Figure 3. L'activation des récepteurs de la dopamine amène une enzyme particulière (de la classe des phospholipases) à découper un précurseur présent dans la membrane des cellules. L'anandamide est ainsi produit et libéré sur commande par les cellules. Son inactivation rapide est assurée par un double processus de recapture et de dégradation : une protéine de transport le véhicule à l'intérieur de la cellule où une enzyme ad hoc le détruit.
Dans quelles régions du système nerveux central a lieu la libération d'anandamide, et dans quelles circonstances ? Une réponse partielle à cette question, qui reste en bonne partie inexplorée, est suggérée par une série d'expériences très récentes, conduites dans notre laboratoire par Andrea Giuffrida, en collaboration avec Loren Parsons (au Scripps Research Institute de San Diego).
Analogie. Nous avons étudié la libération d'anandamide dans le striatum, une région du cerveau qui contient un nombre très élevé de récepteurs cannabinoïdes. En raisonnant par analogie avec d'autres neurotransmetteurs, nous avons supposé que, si l'anandamide joue en rôle de modulation dans cette région, il devrait être produit et libéré lorsque les neurones striataux sont actifs. Pour tester cette hypothèse, il était nécessaire de mesurer le relargage d'anandamide dans des conditions le plus physiologiques possible, ce que nous avons fait en utilisant la microdialyse, une technique qui permet de déterminer les concentrations de différents médiateurs chimiques dans le cerveau d'un animal vivant.
A notre grande surprise, l'activité électrique des neurones striataux ne causa qu'une faible libération d'anandamide. En revanche, le lipide était relargué en quantités très importantes lorsque nous stimulions un sous-type de récepteurs de la dopamine, appelé récepteur D2. Or, les travaux de l'équipe de Jacques Glowinski (au Collège de France) et d'autres scientifiques avaient montré que l'une des fonctions primaires de la dopamine est de faciliter l'activité motrice, un rôle qu'elle exerce en partie grâce à l'activation de ces récepteurs D2 dans le striatum . En montrant que ceux-ci causent la libération d'anandamide, nos données suggéraient donc que le système cannabinoïde pourrait, lui aussi, participer au contrôle du mouvement.
Pour déterminer si cette hypothèse était correcte, nous avions à disposition un outil pharmacologique précieux. En 1994, les scientifiques de Sanofi Recherche à Montpellier ont en effet mis au point un antagoniste sélectif du récepteur cannabinoïde, le composé SR141716A (un antagoniste est une molécule qui se lie très fortement au récepteur sans provoquer son activation, et qui empêche ainsi la fixation d'activateurs). Ce produit nous a permis d'évaluer le rôle de l'anandamide dans le contrôle du mouvement, en collaboration avec Fernando Rodriguez de Fonseca et Miguel Navarro, à l'université Complutense de Madrid.
Un phénomène très intéressant se présenta tout de suite à notre attention : tandis que l'antagoniste cannabinoïde n'avait aucun effet lorsqu'il était administré tout seul, il causait une forte augmentation des mouvements induits par la stimulation du récepteur D2(8). L'interprétation la plus plausible de ces résultats était que l'anandamide relargué par l'activation des récepteurs D2 agit comme un « frein » qui contrôle et régularise l'activité stimulante de la dopamine (fig. 4). La fonction de l'anandamide se révélait par la même partiellement élucidée : moduler finement les effets de ce neurotransmetteur essentiel.

- Figure 4. La dopamine, via les récepteurs de type D2, facilite l'activité motrice en même temps que la synthèse d'anandamide, qui active les récepteurs cannabinoïdes inhibant le mouvement. L'anandamide modulerait, entre autres, les effets de la dopamine sur la motricité.
Cette connexion entre dopamine et anandamide, mise en relief par ces résultats, pourrait nous aider à mieux comprendre certaines affections neuropsychiatriques. Par exemple, on sait que plusieurs maladies mentales - y compris la schizophrénie et le syndrome de Gilles de la Tourette* - sont caractérisées par une activité excessive du réseau de neurotransmission qui utilise la dopamine comme médiateur. Si le système cannabinoïde endogène est mis en jeu par la dopamine, comme nos données le suggèrent, les taux cérébraux d'anandamide devraient être plus élevés chez les individus affligés par ces maladies(9).
Résultats préliminaires. Effectivement, une étude que nous avons conduite récemment en collaboration avec Markus Leweke et Hindrich Emrich, à l'université de Hanovre montre que le liquide céphalo-rachidien* de patients schizophrènes contient une concentration d'anandamide plus élevée que celui de sujets sains. Bien que ces données soient trop préliminaires pour nous permettre de tirer des conclusions définitives, elles suggèrent tout de même que le système cannabinoïde endogène joue un rôle significatif dans certaines maladies mentales, et pourrait être donc choisi comme cible pour des nouveaux médicaments antipsychotiques. L'hypothèse que Moreau de Tours avait formulée en 1845 se révèle confirmée.
Un nouveau médicament. Les applications thérapeutiques possibles de médicaments agissant sur le système cannabinoïde endogène ne se limitent pas au domaine de la neuropsychiatrie. Les propriétés analgésiques du THC et d'autres activateurs des récepteurs cannabinoïdes, auxquelles faisaient déjà allusion les scientifiques du siècle dernier, ont été confirmées par plusieurs études récentes.
En particulier, les travaux de Michael Walker (à la Brown University de New York) et de Howard Fields (à l'université de Californie) ont montré que les dérivés du THC agissent en activant des récepteurs cannabinoïdes présents dans les mêmes régions du cerveau affectées par les opiacés, et produisent des effets antalgiques* tout à fait comparables(10).
Si les propriétés analgésiques des dérivés du THC n'ont pas encore été exploitées thérapeutiquement, c'est principalement à cause de leurs actions psychotropes. Mais, aujourd'hui, la prévention de ces effets collatéraux n'est plus un problème insoluble. Par exemple, des récepteurs cannabinoïdes à fonction analgésique ont été découverts dans la peau et dans d'autres tissus périphériques : il est donc concevable que des molécules de synthèse capables d'activer ces récepteurs extracérébraux d'une façon sélective puissent soulager certaines formes de douleur sans provoquer les inconvénients typiques des cannabinoïdes à action centrale.
De nombreuses données anecdotiques et quelques études cliniques suggèrent que des agents cannabinoïdes à action périphérique pourraient également être employés dans le traitement symptomatique de la sclérose en plaques. La prise de cannabis ou l'administration de THC semblent réduire les spasmes musculaire et la douleur chronique qui caractérisent cette maladie(11).
Contre l'anorexie. Les effets anti-vomitifs du cannabis et sa capacité à stimuler l'appétit ont été confirmés par plusieurs témoignages cliniques, mais les bases neurobiologiques de ce phénomène restent inconnues. De plus, les expériences effectuées sur des modèles animaux n'ont apporté jusqu'à maintenant que des résultats ambigus. Son utilisation dans le traitement de l'anorexie et de la nausée associées avec la prise de médicaments anticancéreux reste envisagée. Il existe par ailleurs une forme grave d'anorexie dans laquelle les agents cannabinoïdes pourraient trouver une application thérapeutique : l' anorexia nervosa, un syndrome neuropsychiatrique qui atteint 1 % des adolescentes et qui est caractérisé par un taux de mortalité très élevé (5% à 18 %).
Les études de Per Södersten et de Cecilia Bergh au Karolinska Institut de Stockholm suggèrent que cette maladie est causée par une activité excessive des mécanismes cérébraux de récompense associés à la dopamine(12). L'activation du système cannabinoïde endogène pourrait être exploitée, comme nous l'avons vu, pour contraster cet état d'hyperactivité dopaminergique et pour corriger ces symptômes.
A l'opposé, si les activateurs du récepteur cannabinoïde stimulent l'appétit, les antagonistes de ce même récepteur devraient exercer un effet contraire, et entraîner une réduction de la prise alimentaire. C'est justement ce qu'a pu constater l'équipe de Gianluigi Gessa (à l'université de Cagliari), à la suite d'une série d'expériences avec l'antagoniste cannabinoïde. L'utilité de cette classe de composés dans le traitement de l'obésité, suggérée par ces données, doit naturellement être confirmée par des essais cliniques.
Il faut toutefois insister sur un point. Les effets psychotropes liés à l'utilisation de composés cannabinoïdes restent un obstacle majeur à leur utilisation thérapeutique. L'identification de récepteurs périphériques aux propriétés différentes de leurs homolgues présents dans le cerveau, et le développement d'outils pharmacologiques qui leur soient propres est une première piste de recherche. La seconde est offerte par les inhibiteurs sélectifs du processus d'inactivation de l'anandamide.
Cette classe de molécules, que notre laboratoire est en train de développer en collaboration avec Alexandros Makriyannis, de l'université du Connecticut, a comme effet primaire de causer une accumulation d'anandamide dans le milieu extracellulaire, ce qui provoque une activation des récepteurs cannabinoïdes limitée aux régions du cerveau où l'anandamide est relarguée. Cette approche permettra peut-être d'identifier de nouveaux outils pharmacologiques avec un spectre d'action plus favorable que les activateurs directes des récepteurs cannabinoïdes.
DANIELE PIOMELLI
Pour en savoir plus
- Bernard Rocques, Les Drogues et leurs dangers, rapport au secrétariat d'Etat à la santé, Editions Odile Jacob, 1998
- Mary Lynn Mathre, Cannabis in Medical Practice : A legal, Historical and Pharmacological Overview of the Therapeutic Use of Marijuana, Mc Farland & Company, 1997.
- Solomon Snyder, La Marijuana, Editions du Seuil, Paris, 1981.
*LA PHILOLOGIE est l'étude historique des textes.
*PHILIPPE PINEL (1745-1826). Médecin à Bicêtre puis à la Salpêtrière, il abolit les méthodes thérapeutiques brutales auxquelles étaient soumis les aliénés. On lui doit, notamment, un Traité médico-philosophique sur l'aliénation mentale ou la manie (1801).
*LE LIQUIDE CÉPHALO-RACHIDIEN baigne le système nerveux central, en deux compartiments interconnectés : l'un, périphérique, entre les méninges et le cerveau et l'autre, central - les ventricules cérébraux.
*LA MALADIE DE GILLES DE LA TOURETTE est caractérisée par des mouvements involontaires (tics), des troubles du langage et mène à une détérioration intellectuelle progressive.
*LES ANTALGIQUES calment la douleur.
(1) Aspects moléculaires cellulaires et physiologiques des effets du cannabis, rapport de l'Académie des sciences, 1997.
(2) B. Roques, Les Drogues et leurs dangers, rapport au secrétariat d'Etat à la Santé Odile Jacob, 1998.
(3) Gaoni et R. Mechoulam, J.A.M. Chem. Soc, 86, 164, 1964.
(4) L.A. Matsuda et al., Nature, 364, 561, 1990.
(5) W. A. Devane et al., Science, 258, 1946, 1992.
(6) V. Di Marzo et al., Nature, 372, 686, 1994.
(7) M. Beltramo et al., Science, 277, 1094, 1997.
(8) A. Giuffrida et al., Nature Neuroscience, 2, 358, 1999.
(9) F.M. Leweke et al., Neuroreport, 10, 277, 1999.
(10) A. Calignano et al., Nature, 394, 277, 1998.
(11) P. Consroe et al., European Neurology, 38, 44, 1997.
(12) P. Södersten et C. Bergh, Lancet, 351, 9113, 1427, 1998.